『緑鉛鉱-黄鉛鉱固溶体の単結晶育成技術の開発とその応用』 ![]()
~アパタイトグループの鉱物の着色現象が示す地球科学的な意味についての研究~
<はじめに>
緑鉛鉱[Pb5(PO4)3Cl]と黄鉛鉱[Pb5(AsO4)3Cl]は、鉛鉱床の酸化帯上部に産する二次鉱物である(Roberts et al. 1990; Clark 1993; Gaines et al. 1997;
Anthony et al. 2000)。両者はアパタイトグループに属し、アパタイトと同じ結晶構造を所持する。主な共生鉱物には、白鉛鉱、硫酸鉛鉱、菱亜鉛鉱、珪亜鉛鉱、モリブデン鉛鉱、方鉛鉱が知られている(Anthony
et al. 2000)。緑鉛鉱は、しばしば黄鉛鉱を伴って産出し累帯構造を形成することも知られており(Clark 1993)、西南北海道小樽松倉重晶石鉱床から発見された緑鉛鉱―黄鉛鉱からは、結晶の中心部から外側に向かって黄色の黄鉛鉱から緑色の緑鉛鉱に変化する累帯構造が観察される(Nakamoto
et al. 1969)。この原因を、Nakamoto et al. (1969)は、結晶が生成しているときの溶液組成の変化であると考えている。つまり、結晶化初期の溶液はヒ酸成分に富んでいたが、それが後期にはリン酸成分に富んだ溶液に変化し、この溶液の組成変化が結晶化の過程で劇的に起こったためであると考えた。さらに、Inegbenebor
et al. (1989)も、実験によって緑鉛鉱―黄鉛鉱の組成変化は水溶液中のリン酸とヒ酸の濃度比の変化を反映したものであるとし、この変化は鉱物の生成環境変化にも適応できると述べている。しかし、ヒ酸やリン酸に富んだ溶液が存在したと仮定した場合、Nakamoto
et al. (1969)も指摘しているように、小樽松倉重晶石鉱床からは、リン、ヒ素を主要に含む鉱物は緑鉛鉱と黄鉛鉱以外には産出していない。また、世界各地の鉛鉱床からも、リン酸塩鉱物、ヒ酸塩鉱物が、緑鉛鉱と黄鉛鉱の共生鉱物として産出することは極めて少ない(Anthony
et al. 2000)。したがって、緑鉛鉱―黄鉛鉱が結晶化するプロセスに、リン酸やヒ酸を含む溶液が大規模に関与したという考え方(Nakamoto
et al. 1969; Inegbenebor et al. 1989)は、極めて懐疑的であると言わざるを得ない。そのため、天然における緑鉛鉱―黄鉛鉱の結晶化メカニズムについては未だに不明な点が多く、緑鉛鉱―黄鉛鉱の生成環境を矛盾なく説明できるような新しい結晶生成モデルの提唱が求められる。

図1. (写真・左) 緑鉛鉱、白色部は重晶石。産地はCordoba, スペイン。(写真・右) 黄鉛鉱、白色部は方解石。産地はSanta Eulalia, メキシコ。スケールは両写真とも写真の一辺が約2cm。
緑鉛鉱―黄鉛鉱は多彩な色を示す; 緑鉛鉱は、濃緑色、薄緑色、褐色、黄色、白色、無色、黄鉛鉱は薄黄色、黄褐色、黄橙色、橙赤色、白色、無色(Roberts
et al. 1990; Gaines et al. 1997)。この二種類が完全固溶体を成すことは、実験からも確認されている(Baker,
1966; Nakamoto et al. 1969)。緑鉛鉱-黄鉛鉱固溶体は天然でも知られており(Adedayo et al. 1989;
Clark 1993)、一般にリンとヒ素を比べてリンが多いときに緑鉛鉱、ヒ素が多いときに黄鉛鉱と呼ばれる(Gaines et al. 1997)。しかし、固溶体と色の関係は、十分に研究が進んでいない。この最大の理由は、緑鉛鉱と黄鉛鉱には、これまで発色を確認出来るサイズまで結晶を成長させる結晶育成法が開発されていないためである。合成実験によって得られた結晶はすべて粉末であり、その色は条痕色を示しているにすぎない(Baker,
1966; Nakamoto et al. 1969)。さらに、緑鉛鉱の結晶育成法として青木ら(1986)が提案した塩化鉛を融剤として用いるフラックス法も、再現性に乏しく有効な方法ではない。また、塩化鉛を用いるため、融剤が水に難溶であり、結晶との分離が困難である。そのため、塩化鉛を融剤とするフラックス法は、色を調べる際に次なる困難を伴う。さらに、近年、Franke
(1996)が、緑鉛鉱の合成方法として、ゲル育成法を提案してたが、成長した結晶の大きさは0.1mmと非常に小さく、詳細な実験方法の記載もない。Franke
(1996)は、ゲル育成法による黄鉛鉱の結晶育成法も提案しているが、こちらも同様に成長した結晶が0.1mmと非常に小さく、詳細な実験方法の記載がない。したがって、このような背景から、従来の合成法からは、緑鉛鉱と黄鉛鉱の発色を確認できるほどの大きさのものを得ることが出来ず、緑鉛鉱―黄鉛鉱固溶体における結晶の発色機構を詳しく調べることが不可能であった。つまり、緑鉛鉱と黄鉛鉱の色の多様性の原因を実験によって調べるためには、従来の単結晶合成法や固溶体合成方法では不可能であり、数mm程度の結晶サイズを確保できる結晶合成方法を新しく確立することが必要なのである。さらに、本研究によって、緑鉛鉱―黄鉛鉱の多様な色の原因の一端を解明することができれば、同構造であり同じように多様な発色を示す燐灰石の色の多様性についての原因究明にもなる。
以上のような研究背景から、本研究では次の二つの研究目的を設定した。第一の目的は、緑鉛鉱―黄鉛鉱の生成環境を考察するため、緑鉛鉱、黄鉛鉱の結晶成長に最も適当な結晶育成方法を開発すること。そして、第二の目的は、その合成方法を確立して、緑鉛鉱―黄鉛鉱の端成分、固溶体結晶を育成し、発色機構と固溶関係について考察することである。
<実験方法>
出発物質の合成には、Baker(1966)の方法を参考にした。彼の方法から、目的とする緑鉛鉱―黄鉛鉱固溶体組成の粉末を合成した。
アパタイト(燐灰石)では、塩化ナトリウムフラックス(融剤)を用いた、塩素燐灰石、バリウム塩素燐灰石、ストロンチウム塩素燐灰石の単結晶育成に成功している(Oishi et al. 1997; 1999; 2001)。結晶の大きさは、それぞれ最大4.0mm、12.0mm、8.6mmである。したがって、本研究ではこの方法を応用し、融剤にはアルカリ塩化物を選択した。実際に使用した融剤は、塩化ナトリウム、塩化リチウム、塩化セシウムの3種類である。しかし、予備実験として塩化ナトリウムや塩化リチウムを用いて合成を行なった結果、緑鉛鉱や、黄鉛鉱の結晶性の物質を得ることは出来なかった。それに対し、塩化セシウムを融剤に使用したところ、数mmサイズの自形の単結晶を得ることに成功した。その後、より良質で大きな単結晶を得ることを目的に、融剤と溶質の割合を変えながら実験を続け、出発物質の融剤に対する溶質濃度を1モル%、2モル%、3モル%として行なった。
出発物質と融剤は、容積30mlの白金るつぼに入れ、しっかり蓋をして電気炉に投入した。実験中は、炉内に不活性ガス(窒素)を流しながら結晶を育成した。温度プログラムは、室温から900℃まで45℃/hで加熱、その後、900℃で5時間保持し、5℃/hで500℃まで徐冷、その後、自然放冷した。冷却後、白金るつぼを取り出し、るつぼ内の融剤を水で溶かし、生成物を分離した。
<結果と考察>
本研究で使用した融剤のうち、塩化ナトリウムでは結晶性物質は得られなかった。Oishi et al. (1997)は、塩素燐灰石に対する最適な融剤として塩化ナトリウムを使用したが、塩素燐灰石の融点は、熱分析の結果、1400℃を超える。塩化ナトリウムは、融点800℃、沸点1413℃である。しかし、緑鉛鉱の融点は約1100℃であり、塩素燐灰石より300℃以上も低い。そのため、塩化ナトリウムは、緑鉛鉱―黄鉛鉱に対する融剤としては溶融温度領域が高く、育成温度も高すぎたために、緑鉛鉱―黄鉛鉱固溶体結晶が得られなかったと考えられる。
塩化リチウムは、融点606℃、沸点1382℃である。この溶融温度領域は、緑鉛鉱や黄鉛鉱には適当である。しかし、得られた結晶はリチウムリン酸塩とリチウムヒ酸塩(図2)であった。これは、リチウム陽イオンが鉛イオンに比べて非常に小さいため、融剤と溶質が反応してしまった結果である。

図2. リチウムリン酸塩(右)とリチウムヒ酸塩(左)。スケールは1mm。
塩化セシウムは、融点645℃、沸点1290℃で、溶融領域が塩化ナトリウムより約150℃低い。また、鉛陽イオンのイオン半径が1.29Åであるのに対し、セシウムのイオン半径は1.74Åであり、溶質と融剤が反応する可能性は低い。これらの諸特性を考慮し、塩化セシウムを融剤として選択した結果、良質の単結晶を得ることが出来た(図3)。さらに、青木ら(1986)が使用した水に難溶な塩化鉛融剤に対し、塩化セシウムは水に易溶であり、結晶と融剤の分離も極めて容易である。また、結晶サイズも彼らの方法のものに比べてはるかに大きく、単結晶育成法としては、本研究の方法の方が明らかに優れている。

図3. 緑鉛鉱、黄鉛鉱の単結晶。溶質濃度緑鉛鉱 (a) 1モル%、(b) 2モル%、(c) 3モル%。黄鉛鉱 (d) 1モル%、(e) 2モル%、(e)
3モル%。スケールは1mm。単結晶のサイズは、溶質濃度3モル%のものが最大となり、最も大きいもので、緑鉛鉱では6.5 x 1.5 mm、黄鉛鉱では8.0
x 1.0 mmのサイズまで成長した。
さらに、塩化セシウム融剤を使用し、端成分の単結晶を育成したときと同じ合成条件で、固溶体の単結晶育成を行なった。今回の融剤に対する出発物質の溶質濃度は1モル%とした。実験の結果、5つの異なる化学組成比のすべてにおいて、単結晶育成に成功した(図4)。したがって、今回の結晶育成方法では、緑鉛鉱―黄鉛鉱固溶体の任意の化学組成における単結晶を育成することが可能であることが判明した。

図4. 結晶育成した緑鉛鉱―黄鉛鉱固溶体結晶。出発物質の緑鉛鉱黄鉛鉱の混合比はそれぞれ、(a) 9:1、(b) 7:3、(c) 5:5、(d)
3:7、(e) 1:9。スケールは1mm。
これまでに、緑鉛鉱―黄鉛鉱固溶体は、合成実験から完全固溶体を形成することが示されていた(Baker 1966; Nakamoto et al.
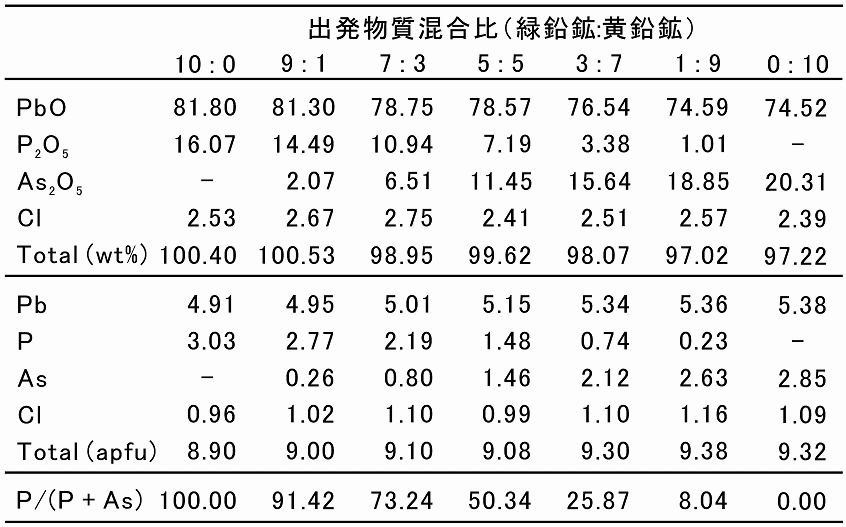
1969)。しかし、過去の実験データは合成物が粉末状であり、結晶の化学組成が測定されていない。今回の実験によって得られた固溶体の結晶を、EPMAで分析した結果、合成結晶は出発物質の化学組成をそのまま維持し、任意の割合でリンとヒ素を固溶できることが判明した(表1)。したがって、緑鉛鉱―黄鉛鉱固溶体が、結晶においても完全な固溶体を形成することが初めて確認された。
表1. EPMAによる分析値。出発物質の混合比がほぼそのまま育成した結晶の化学組成になる。
緑鉛鉱、黄鉛鉱を窒素雰囲気下で結晶育成したときには、端成分ならびに固溶体の結晶はすべて無色透明であった。ところが、電気炉内への窒素ガスの流入を停止し、電気炉内を酸化環境にして、同条件で結晶を育成すると、それによって得られる結晶には、無色透明のものに混じって、黄色に着色した結晶が含まれるようになった。着色した結晶の大きさや形体は、無色透明のものとほぼ同じである(図5)。

図5. 雰囲気による着色の違い。(a) 窒素雰囲気下で育成した黄鉛鉱結晶、(b) 酸素存在下で育成した黄鉛鉱結晶、(c) 窒素雰囲気下で育成した緑鉛鉱5対5黄鉛鉱結晶、(d)
酸素存在下での育成した緑鉛鉱5対5黄鉛鉱結晶。スケールは1mm。
黄色の黄鉛鉱端成分の無色透明結晶と黄色に着色した結晶を選別して、それぞれを分析した。粉末X線回折パターンと格子定数を比較した結果、両者から有意な差を見つけることは出来なかった。また、EPMAによって、微量元素の混入の影響を調べた。その結果、EPMAの検出限界レベルでの微量元素の影響は確認できなかった。さらに、EPMAによる線分析によって、両者の主要元素の特性X線の強度をそれぞれ比較したところ、有意な差は確認できなかった。 さらに 、XPSによって、微量元素と軽元素の影響を調べたが、この結果からも、有意な差は見られなかった。また、IRスペクトル分析の結果からも、明瞭な違いは発見できなかった。したがって、本研究では、窒素を停止した酸素存在下では着色結晶を含むようになることから、着色要因は酸素であると考えた。
石川(2004)は、雰囲気制御下で水酸アパタイトの着色現象について研究を行なった。彼は、電気炉内雰囲気を酸素、窒素、アルゴンで充填し、常温時の圧力を0.006、0.013、0.025、0.050、0.075、0.100、0.125MPaに調節し、水酸アパタイトを1200℃で焼成して着色した焼結体の色を定量した。その結果、赤色に着色した焼結体の彩度は、酸素雰囲気下で最大で、それは、酸素分圧の上昇とともに増加していた。また、石川(2005)は、吸着酸素の定量も行なった。その結果、赤色焼結体には、約0.2~0.4質量%の酸素分子が吸着してた。
本研究では、XPSによって、酸素の結合エネルギー(O1s)を測定して、緑鉛鉱―黄鉛鉱の酸素の効果を調べた。その結果、O1sの結合エネルギーと着色現象に、はっきりとした相関が確認できた。窒素雰囲気下の無色の結晶のピークが530.65 eVであるのに対し、酸素雰囲気下で黄色に着色した結晶の方は、530.73 eVと高エネルギー側にシフトしている(図6)。さらに、天然の緑鉛鉱と黄鉛鉱は、531.44 eV、531.11 eVと(図6)、合成した無色、および着色したのものよりさらに高い値を示した。この現象は、酸化―還元で変色する燐光体でも、酸化環境ではO1sスペクトルは高エネルギー側にシフトすることが確認されている(Kim et al. 2003)。
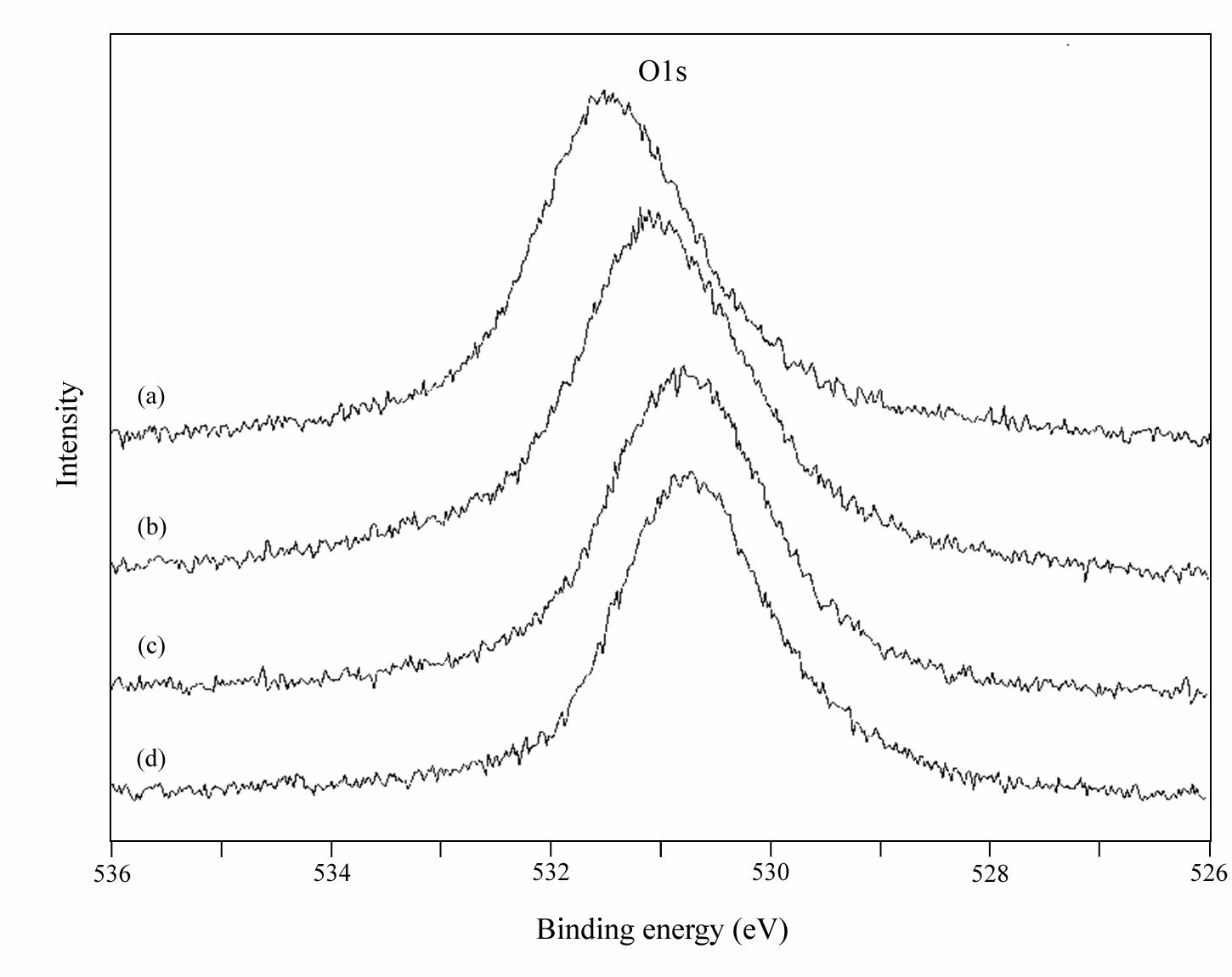
図6. XPSによるO1sスペクトル。(a) 天然緑鉛鉱、(b) 天然黄鉛鉱、(c) 黄色着色結晶 (出発物質比 緑鉛鉱5対5黄鉛鉱)、(d) 無色透明結晶 (出発物質比 緑鉛鉱5対5黄鉛鉱)
つまり、緑鉛鉱や黄鉛鉱は、本来は無色透明であり、天然にみられる多彩な色は、生成時の酸化環境を反映したものであると推察できる。本来、緑鉛鉱、黄鉛鉱の粉末は白色で、条痕色も白色である。これは、合成粉末でも同じである。つまり、天然の緑鉛鉱、黄鉛鉱は、実際には結晶化する時の酸化環境の影響によって、緑色や黄色などに着色している。これは、この鉱物が、一般的に鉛鉱床の酸化帯に産する二次鉱物として知られていることからも(e.g. Clark 1993; Gaines et al. 1997; Anthony et al. 2000)、生成環境場には酸素が存在していることを裏付けている。この影響を受けて、緑鉛鉱―黄鉛鉱固溶体は多彩な色を発現している。したがって、天然で稀に観ることができる無色透明の緑鉛鉱、黄鉛鉱こそ、それらの本質的な色なのである。
謝辞: 本研究は、正岡幹雄君の筑波大学第一学群自然学類における平成17年度卒業研究発表の一部を整理したものである。本研究を進めるにあたり、筑波大学大学院生命環境科学研究科地球進化科学専攻木股三善教授には、大変有益なご助言を頂いた。XPS、FTIRの測定では、独立法人国際農林水産業研究センターの八田珠郎博士、根本清子さんにご協力頂いた。筑波大学研究基盤総合センター分析部門の西田憲正博士には、EPMAの測定で適切なご助言を頂いた。筑波大学生命環境支援室の清水雅浩技官には、分析の技術に加え、研究に対する様々なご助言とご協力を頂いた。筑波大学大学院生命環境科学研究科木股三善研究室の越後拓也さん、星野美保子さん、石田直哉さん、龍徹さんには終始有益なご助言ならびにご協力を頂いた。以上の方々に
ここに厚くお礼申し上げる。また、本研究の一部は、池谷科学技術振興財団、及び日本板硝子材料工学助成会の研究助成金の援助を受けて行なわれたものである。
●詳しく知るには:
・Mikio Masaoka, Atsushi Kyono, Tamao Hatta and Mitsuyoshi Kimata: Single
crystal growth of Pb5(PxAs1-xO4)3Cl solid solution with apatite type structure. Journal of Crystal Growth,
, 292, 129-135, 2006.