 Crystal structure change in the grossular-Si-free katoite solid solution: Oxygen position splitting in katoite 灰礬柘榴石-無ケイ素加藤石固溶体における結晶構造変化: 加藤石内での酸素位置のスプリット 興野純,Shubhi Arora Journal of Mineralogical and Petrological Sciences, 114, 189-200, 2019 |
||||||||||
| 【はじめに】 上部マントルのカンラン石,輝石,柘榴石や,それらの高圧多形は少量の水素を含むことができる.通常は無水であることから,これらは”名目上の無水鉱物”Nominally Anhydrous Minerals (NAMs)と呼ばれている.NAMsによって潜在的には大量の水がマントルに保持されるため,NAMsの研究は地球物理学的にも非常に重要なテーマとなっている.中でも,Si4+と4つのH+が置換するハイドロガーネット(含水柘榴石)置換(SiO4 ⇔ H4O4)は,最も効率よく水素をケイ酸塩鉱物に取り込むことが出来るメカニズムとして広く認められている.そのため,柘榴石はその豊富さと安定性から,地球のマントルで最も重要な水素貯蔵庫の1つと見なされている.ハイドログロッシュラー(含水灰礬柘榴石)[Ca3Al2(SiO4)3-x(H4O4)x (0 < x < 3)]では連続的にハイドロガーネット置換が起きることが知られており,グロッシュラー(灰礬柘榴石)成分が50%以上のものがヒブシュ石(hibschite),50%未満のものが加藤石(katoite)である(Passaglia
& Rinaldi, 1984).ハイドログロッシュラーの固溶体の研究は,1940年代から行われており(Flint et al., 1941),加藤石側の組成に不混和領域が存在している可能性が多くの研究者によって指摘されている(Shoji,
1974; Jappy and Glasser, 1991; Bennett et al., 1992; Kyritsis et al., 2009;
Dilnesa et al., 2014).例えば,Kyritsis et al. (2009)は,200℃から350℃の水熱合成実験から,ハイドログロッシュラーの不混和領域は,加藤石側のCa3Al2(H4O4)3からCa3Al2(SiO4)0.8(H4O4)2.2であることを示した.また,最近では,Dilnesa et al. (2014)が,20℃の水和実験によって加藤石側のCa3Al2(SiO4)0.41(H4O4)2.59からCa3Al2(SiO4)0.84(H4O4)2.16に不混和領域が存在していることを示している.さらに,加藤石はハイドロガーネット置換によって対称性が立方晶系から低下することが,第一原理計算によって予想されている(Lacivita
et al., 2015; Adhikari et al., 2017).そのため,ハイドログロッシュラーにおいてケイ素を含む加藤石側については,不混和領域の存在や結晶成長の条件,さらにそれらと結晶構造との関係など,ケイ素を含まない加藤石[Ca3Al2(H4O4)3]に比べて非常に複雑であり不明な点も多く,天然のハイドログロッシュラーの研究も少ない.そこで本研究は,ケイ素を含む加藤石の合成を試み,結晶構造解析から加藤石の構造特性を調べる実験を行った. 【実験方法】 合成実験は,CaとAl源はそれぞれCaOとAlを出発物質として用い,Si源には二種類の出発物質として非晶質シリカ(SiO2)とテトラメチルシラン(Si(CH3)4)を用いた.まず,CaO:Al:SiO2を3:2:1のモル比で混合し蒸留水と共にテフロン容器に入れ250℃,4日間の条件で水熱合成した.続いて,CaO:Alを3:2で混合した粉末を約180mg秤量しテトラメチルシラン約1gと混合し蒸留水と共にテフロン容器に入れて250℃,4日間の条件で水熱合成した.得られた結晶は,単結晶X線回折法(Bruker AXS SMART APEX II ULTRA),ラマン分光法(JASCO NRS-5100),EPMA(JEOL JXA-8530F)によって分析した. 【結果と考察】 合成実験から得られたハイドログロッシュラーは,Si源が非晶質シリカの場合は,約10μm程度の微小な大きさだったのに対し,テトラメチルシランの場合は,約100μmサイズの正八面体型の非常に大きな単結晶が得られた(図1).また,Si源が非晶質シリカの場合は,ハイドログロッシュラーにSiO4成分が最も固溶した化学組成でもCa3Al2(SiO4)0.26(H4O4)2.74であったのに対して,テトラメチルシランの場合は,最大でCa3Al2(SiO4)0.69(H4O4)2.31ものSiO4成分が固溶した.このように本研究では,Kyritsis et al. (2009)が示した不混和領域の組成範囲内においてハイドログロッシュラーを合成することに成功した(図2).このことは,グロッシュラーから無ケイ素加藤石の間には不混和領域は存在せず,完全な連続固溶体になることを示しており,これまでの研究者によって示唆された不混和領域は,主に出発物質にその原因があると考えられる.プリセッション写真からは,本研究で合成されたハイドログロッシュラーはすべて空間群Ia-3dの消滅則を満たしていた.したがって,第一原理計算から予想されていた立方晶系からの対称性低下は見られなかった.ところが,本研究で得られた単結晶のうち,化学組成がCa3Al2(SiO4)0.57(H4O4)2.43とCa3Al2(SiO4)0.69(H4O4)2.23の試料では,酸素原子位置が二つの非等価な位置にスプリットしていた(図3).差フーリエ電子密度図(Fobs-Fcal)の酸素原子周囲に見られる正の残差は,加藤石内の水素原子を示している(図4).ラマン分光スペクトルも酸素原子位置のスプリットを示唆する結果が得られた.これまで加藤石は,ハイドロガーネット置換によってH+とSi4+が置換したした場合は,Siは加藤石の空隙である四面体席に分配され両者は等価な位置に無秩序配置され区別できないと考えれれていた.しかし,本研究の結果は,酸素原子が二種類の非等価な位置にスプリットして,Siによって占有されるSiO4配置と空隙からなるH4O4配置の2種類の異なる配位環境に完全に分かれることを示した(図5). ●参考文献 Dilnesa, B.Z., Lothenbach, B., Renaudin, G., Wichser, A., and Kulik, D. (2014) Synthesis and characterization of hydrogarnet Ca3(AlxFe1-x)2(SiO4)y(OH)4(3-y). Cement and Concrete Research, 59, 96-111. Kyritsis, K., Meller, N., and Hall, C. (2009) Chemistry and morphology of hydrogarnets formed in cement-based CASH hydroceramics cured at 200o to 350oC. Journal of American Ceramic Society, 92, 1105-1111. Lacivita, V., Mahmoud, A., Erba, A., D'Arco, P., and Mustapha, S. (2015) Hydrogrossular, Ca3Al2(SiO4)3–x(H4O4)x: An ab initio investigation of its structural and energetic properties. American Mineralogist, 100, 2637-2649.
|
 図1. 加藤石の単結晶.出発物質のSi源が(a)非晶質シリカと(b)テトラメチルシラン. 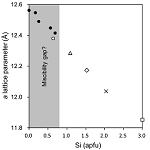 図2. 格子定数の変化. 合成加藤石はKyritsis et al. (2009)の不混和領域の化学組成を示す. 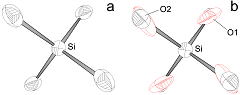 図3. 四面体配位のOrtep. (a)非スプリット配置と(b)スプリット配置 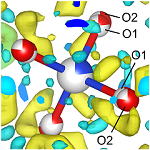 図4. 差フーリエ電子密度図.黄色が正の残差. 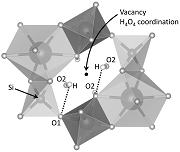 図5. 加藤石の結晶構造. SiO4配置とH4O4配置に分かれる. |
|||||||||
| Copyright © 2004-2025 Atsushi Kyono. All Rights Reserved. | ||||||||||
